查尔斯定律计算器
查尔斯定律计算器使用查尔斯定律公式进行计算,该公式计算理想气体在恒定压力下的初始体积和最终体积以及温度值。
V1 / T1 = V2 / T2
查尔斯定律
查尔斯定律是一种实验气体定律,它涉及当压力保持恒定时接近理想气体的固定质量气体的体积和温度。该定律以科学家雅克·查尔斯的名字命名,他首先制定了原始法律。
查尔斯定律的现代表述指出,当干燥气体样品上的压力保持恒定时,开尔文温度和体积将成正比。这种直接比例关系可以写成以下查尔斯定律公式:
•V 是气体的体积,
•T 是气体的温度(以开尔文为单位),
•k 是一个非零常量。
查尔斯定律通常以以下形式表示:
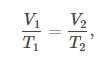
•V1 是初始体积,
•T1 是初始温度(以开尔文为单位),
•V2 是最终体积,
•T2 是最终温度(以开尔文为单位)。
应该强调的是,上述公式使用以开尔文为单位测量的温度。回想一下,开尔文是温度的 SI 单位,有时也称为绝对温度。如果要使用其他温度单位,则必须使用以下转换公式:
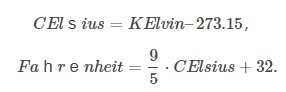
当您使用我们的查尔斯定律计算器并选择所需的单位时,这些转换会自动完成。
使用查尔斯定律时,请记住它仅适用于接近理想气体的气体。理想的气体由尺寸可以忽略不计的颗粒组成,这些颗粒彼此不相互作用。理想的气体模型很容易理解查尔斯定律的物理含义。
事实上,气体温度的升高会导致单个气体分子移动得更快。分子移动得越快,它们与气体容器壁碰撞的频率和力度就越大。更频繁和更有力的碰撞会导致更高的压力。但是,如果容器的容积可调,则容积将在压力保持不变的同时增加。系统中的压力保持恒定的热力学过程称为等压。
发生这种情况是因为,尽管分子的平均速度增加,但与壁碰撞的频率降低。反过来,这是由于体积增加,分子在与壁碰撞之前的平均路径长度增加。结果,压力保持恒定。
当气体温度降低时,会发生相反的过程。从上面的公式可以看出,当温度降低到零时,气体的体积也趋于零。0 K = -273.15 ºC的温度称为绝对零度。根据经典物理学,在这个温度下,所有的运动都停止了。很明显,在这个温度下,由没有大小的颗粒组成的理想气体的体积将为零。